
LPSの基礎知識
(6)リーキーガットとLPS
多くの本や雑誌等でリーキーガットの説明として、しばしば腸内のLPSが原因で起こるかのように記載されているのを見受けますが、LPSは健康な人の腸内にも常に存在していて、リーキーガットの直接的要因となることはありません。
以下、リーキーガットについて興味のある方はお読みください。
<腸壁バリア>
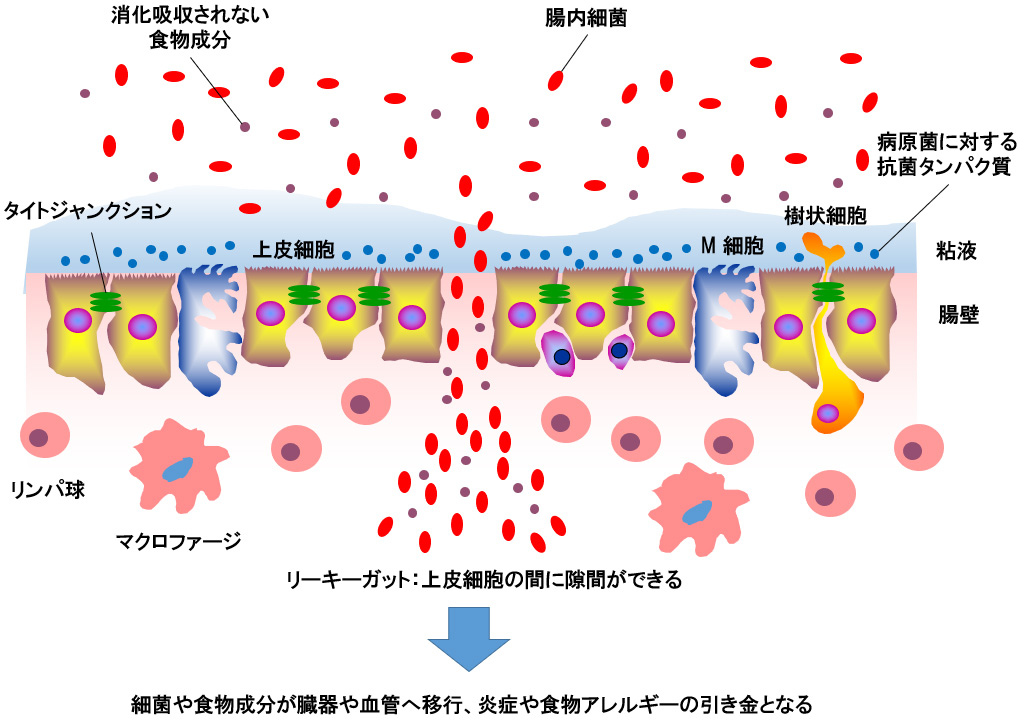
腸は、食物の消化と栄養素の吸収を行う器官ですが、消化吸収されなかった食物成分、常在細菌、病原菌など、非常にたくさんの雑多な物質が通過あるいは滞留するところです。従って腸壁には、必要な栄養素を吸収しつつも体の中に入れてはいけないものをブロックするという特別なバリアシステムが存在します。このバリアシステムは、物理的には、腸壁を作っている上皮細胞が担っており、上皮細胞の間隙はタイトジャンクション(タンパク質からできている)がぴったりシールしています。このバリアには、上皮細胞からムチンのような粘性のある糖タンパク質や、病原菌を寄せ付けないための抗菌物質が出ています。
<リーキーガットとは>
ところで、何らかの原因で上皮細胞の間隙をシールするタイトジャンクションが緩むと、バリアシステムが破たんし、腸内にあるべきものが上皮細胞間の隙間をすり抜けて、体の中に入って行きます。これがリーキーガット(漏れる腸)と呼ばれる現象です。
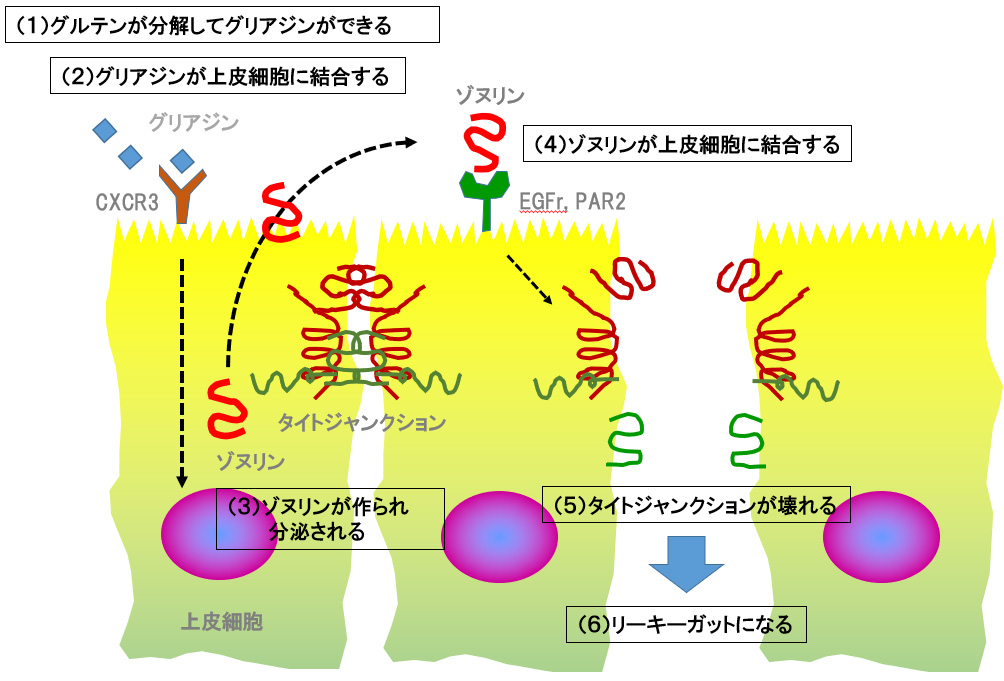
<リーキーガットの原因>
リーキーガットの原因として良く知られているのが、小麦タンパク質であるグルテンです。グルテンの分解物であるグリアジンが上皮細胞に結合すると、上皮細胞内に信号が送られゾヌリンというたんぱく質が過剰に分泌されます。分泌されたゾヌリンは、上皮細胞自身に改めて結合して信号を送り、その結果、タイトジャンクションを形成しているタンパク質どうしの結合がほどけるのです(*1, *2)。グルテンのほかにも、タイトジャンクションを弱める作用のある食品成分として、アルコール(エタノール)、キトサン、カプシアノサイド(唐辛子成分)などが報告されています(*3)。食品による直接的効果のほか、繊維質の少ない食事や火傷のようなストレスによって起こる腸内細菌バランスの変化によってもリーキーガットが引き起こされることが報告されています(*4、*5)。
<リーキーガットになると>
リーキーガットになると、食物成分や細菌が体の中に漏れていきます。腸管では無害に存在する食物成分は、体の中では外来異物と認識されて抗体がつくられ、抗体ができることが食物アレルギーのきっかけとなります(*1, *2)。また食物成分や、腸内では仲間としての位置づけの腸内細菌も、体の中に移行すると、免疫系から外来異物として攻撃を受けて、そこに炎症が起こります。もし原因が取り除かれずに持続すればリーキーガットが慢性的に引き起こされ、慢性的に炎症が続きます。リーキーガット由来の慢性的炎症は、糖尿病、高脂血症や肥満、認知症の進行を促進すると言われています。
<リーキーガットとLPS>
グラム陰性細菌の種類が体の中に入った時、グラム陰性細菌の持つLPSは、強く炎症を誘導します。このことは良く知られた事実です。ただし、健常な人の腸管その他の消化管や皮膚においてLPSが炎症を起こすことはありません。多くの本や雑誌等でリーキーガットの説明として、しばしば腸内のLPSが原因で起こるかのように記載されているのを見受けますが、LPSは健康な人の腸内に常に存在していて、リーキーガットの直接的要因となることはありません。上述したように、腸内は通り過ぎる食物も体の中に入ると異物とみなされて食物アレルギーを引き起こします。LPSも体の中に入ったときに危機のシグナルとして炎症を起こすのです。口から摂取して消化管に入るLPSを危険視する必要は全くありません。逆に、火傷によってリーキーガットが起こった際の、病原菌の体内移動がLPSの経口摂取で抑制されると言う論文もあります(*6)。また、薬剤(硫酸デキストランナトリウム:DSS)でリーキーガットを誘導する動物モデルにおいて、血液中のLPSレベルは上昇しないことや(*7)、むしろ腸内細菌由来のLPSが腸管の恒常性維持と保護に必要であることを示した論文もあります(*8)。
<リーキーガットは治るか?>
リーキーガットは治らないのか?というと、上述したようにもともとリーキーガットは炭水化物(グルテン)過多や繊維質不足のように偏った食事や、強いストレスが原因で起こりますから、食事を見直して腸内細菌バランスを整えること、そしてストレスを発散させることで治る可能性が高いです。
(*1) Gliadin, zonulin and gut permeability Effects on celiac and non-celiac intestinal mucosa and intestinal cell linesScandinavian Journal of Gastroenterology, 41: 408-419 (2006)Scandinavian
Journal of Gastroenterology, 41: 408-419 (2006)
(*2) Zonulin and its regulation of intestinal barrier function:The biological door to inflammation, autoimmunity, and cancer.
Phisiol Rev. 91: 151-175 (2011) (2011)
(*3)Nutritional Keys for intestinal Barrier Modulation
Frontiers in Immunology, 6: Article 612
(*4)A dietary fiber-deprived gut microbiota degrades the colonic mucus barrier and enhances pathogen susceptibility.
Cell, 17; 167(5): 1339–1353 (2016)
(*5)Burn injury alters the intestinal microbiome and increases gut permeability and bacterial translocation
PLOS One|DOI:10,1371/journal.pone.0129996 (2015)
(*6)Commensal microflora induce host defense and decrease bacterial translocation in burn mice through toll-like receptor 4
Journal of biomedical Science, 17:48 (2010)
(*7)Inadequate clearance of translocational bacterial products in HIV-infected humanized mice.
PLoS Pathog 6(4): e1000867. doi:10.1371/journal.ppat.1000867 (2010)
(*8)Recognition of commensal microflora by toll-like receptors is required for intestinal homeostasis.
Cell, Vol. 118, 229–241, July 23 (2004)


